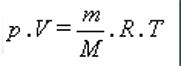|
The ideal gas law relates physical conditions as follows: P V = n R T where
|
De ideale-gaswettoestandsvergelijking van een ideaal gasDe toestand van een hoeveelheid van n mol van een ideaal gas kan worden beschreven met de variabelen: druk, volume en temperatuur. Het verband tussen deze variabelen wordt gegeven door de ideale-gaswet: p . V = n . R . T
Ga na dat links en rechts van het =-teken dezelfde eenheden staan; bedenk daarbij wat de eenheden Pa en J eigenlijk voorstellen. In woorden kun je de ideale-gaswet formuleren als bijvoorbeeld:
|
Een handiger formuleringWanneer niet de hoeveelheid gas in mol, maar de massa ervan (in g) gegeven is, wordt de formulering van deze wet:
|